Risk factors of intraoperative hypothermia in patients undergoing radical thyroidectomy under laparoscopy and the construction of nomogram model
-
摘要:目的
分析腔镜下甲状腺癌根治术患者术中低体温的危险因素并构建列线图预测模型。
方法选取336例腔镜下甲状腺癌根治术患者作为研究对象, 根据术中体温分为低体温组195例和正常体温组141例。采用Logistic回归模型分析腔镜下甲状腺癌根治术患者术中低体温的危险因素,再利用R软件构建列线图预测模型,通过受试者工作特征(ROC)曲线、校准曲线、Hosmer-Lemeshow拟合优度检验评估列线图预测模型的预测效能。
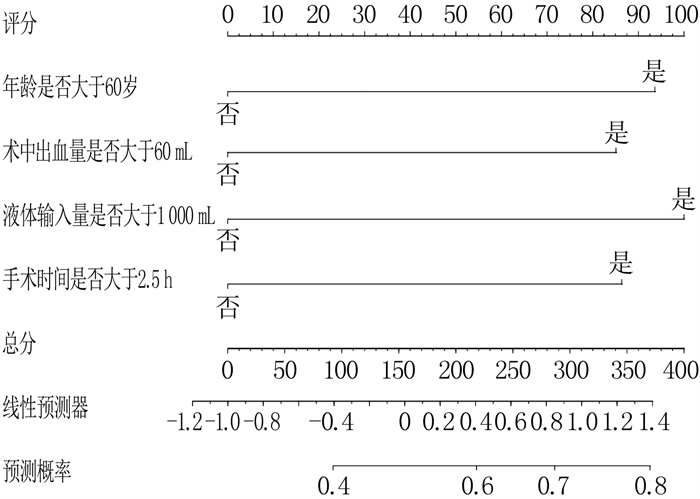
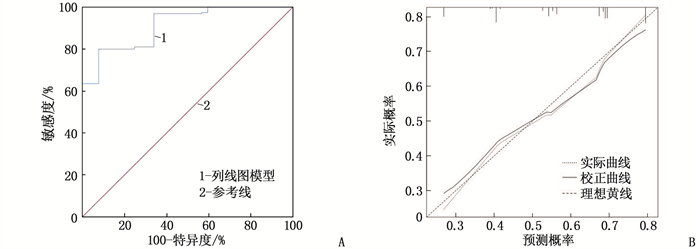
结果2组患者的年龄、术中出血量、液体输入量、手术时间比较,差异有统计学意义(P < 0.05); 多因素Logistic回归分析结果显示,年龄>60岁、术中出血量>60 mL、液体输入量>1 000 mL、手术时间>2.5 h为腔镜下甲状腺癌根治术患者术中低体温的危险因素(P < 0.05); 依据4项危险因素构建列线图预测模型,ROC曲线显示曲线下面积为0.912(95%CI: 0.884~0.941), 校准曲线、Hosmer-Lemeshow拟合优度检验结果显示校准曲线斜率接近1(χ2=9.140, P=0.243)。
结论基于年龄、术中出血量、液体输入量、手术时间构建的列线图预测模型,对腔镜下甲状腺癌根治术患者术中低体温具有较好的预测价值。
-
关键词:
- 腔镜下甲状腺癌根治术 /
- 低体温 /
- 危险因素 /
- 列线图模型 /
- 出血
Abstract:ObjectiveTo analyze the risk factors of intraoperative hypothermia in patients undergoing radical thyroidectomy under laparoscopy and to construct a nomogram prediction model.
MethodsA total of 336 patients who underwent laparoscopic radical thyroidectomy were selected as study subjects. According to intraoperative body temperature, they were divided into hypothermia group (195 cases) and normal temperature group (141 cases). The risk factors of intraoperative hypothermia in patients undergoing laparoscopic radical thyroidectomy were analyzed using the Logistic regression model. The nomogram prediction model was constructed using R software. The prediction performance of the nomogram prediction model was evaluated using the receiver operating characteristic (ROC) curve, calibration curve, and Hosmer-Lemeshow goodness-of-fit test.
ResultsThere were significant differences in age, intraoperative blood loss, amount of fluid infusion, and operation time between the two groups (P < 0.05). Multivariate Logistic regression analysis showed that age>60 years, intraoperative blood loss >60 mL, amount of fluid infusion>1 000 mL, and operation time>2.5 h were risk factors for intraoperative hypothermia in patients undergoing laparoscopic radical thyroidectomy (P < 0.05). A nomogram prediction model was constructed based on the four risk factors. The ROC curve showed that the area under the curve was 0.912 (95%CI, 0.884 to 0.941). The calibration curve and Hosmer-Lemeshow goodness-of-fit test showed that the slope of the calibration curve was close to 1 (χ2=9.140, P=0.243).
ConclusionThe nomogram prediction model based on age, intraoperative blood loss, amount of fluid infusion, and operation time has good predictive value for intraoperative hypothermia in patients undergoing laparoscopic radical thyroidectomy.
-
Keywords:
- laparoscopic radical thyroidectomy /
- hypothermia /
- risk factors /
- nomogram model /
- hemorrhage
-
症状性颅内动脉狭窄(sICAS)是指由动脉粥样硬化引起的颅内动脉狭窄,且狭窄动脉供血区域发生过缺血性卒中或短暂性脑缺血发作[1-2]。研究[3-4]显示,1/3~1/2的缺血性卒中病例与sICAS有关。血管内支架置入术作为一种微创治疗方法,因能迅速改善大脑供血、创伤小且安全性较高,已成为治疗sICAS的主要手段[5]。然而,由于颅内血管结构复杂,支架置入过程中可能存在较高的并发症风险[6]。本研究探讨血管内支架置入术治疗sICAS患者的安全性及有效性,以期为sICAS的临床治疗提供参考依据。
1. 资料与方法
1.1 一般资料
选取北京京煤集团总医院2021年9月—2023年11月收治的100例sICAS患者作为研究对象。纳入标准: ①经影像学检查确诊sICAS者; ②临床资料完整者; ③签署知情同意书者。排除标准: ①合并颅内动脉瘤、蛛网膜下腔出血等脑血管疾病者; ②严重凝血功能异常者; ③合并精神疾病者; ④过敏体质或存在支架置入禁忌证者。采用随机数字表法将患者分为对照组和研究组,每组50例。对照组男28例,女22例; 年龄41~78岁,平均(62.31±6.52)岁; 体质量指数为(22.64±2.23)kg/m2; 颅内动脉狭窄率为(85.87±4.52)%。研究组男26例,女24例; 年龄43~77岁,平均(61.65±5.57)岁; 体质量指数为(22.51±2.30) kg/m2; 颅内动脉狭窄率为(85.23±5.47)%。2组患者基线资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
对照组采用规范药物治疗方案: 口服阿司匹林肠溶片(100 mg/次, 1次/d)、氯吡格雷(75 mg/次, 1次/d)抗血小板聚集,口服阿托伐他汀钙片(10 mg/次, 1次/d)降低血脂和稳定斑块,口服氨氯地平等降压药物稳定血压(目标血压为收缩压130~150 mmHg, 舒张压70~80 mmHg, 1 mmHg=0.133 kPa)。
研究组采用血管内支架置入术治疗方案: 术前3 d口服拜阿司匹林(100 mg/次, 1次/d)、氯吡格雷(75 mg/次, 1次/d); 全身麻醉或局部麻醉下,经股动脉穿刺置管,并进行全身肝素化; 通过数字减影血管造影(DSA)确定狭窄血管病变处,并评估狭窄程度; 使用常规微导丝携带微导管至血管病变远端; 将球囊送至狭窄段,进行扩张; 扩张后,置入支架; 支架置入成功后,通过血管造影再次评估狭窄情况; 术后给予患者低分子肝素治疗3 d,并针对危险因素或手术并发症等不良事件采取相应处理措施。
1.3 观察指标
① 2组患者治疗前和治疗后14 d的颅内动脉狭窄率; ② 2组患者治疗前和治疗后14 d的神经功能,采用美国国立卫生研究院卒中量表(NIHSS)评估,总分42分,评分越高表示神经功能损伤越严重; ③ 2组患者治疗前和治疗后14 d的日常生活能力,采用日常生活活动能力量表(ADL)评估,总分100分,评分越高表示日常生活活动能力越好; ④ 2组患者治疗前与治疗后14 d的脑血流灌注指标,包括狭窄段收缩期峰值流速(PSV)和搏动指数,通过经颅彩色多普勒超声(TCCD)测量; ⑤ 2组患者不良反应发生情况,包括缺血性卒中、出血性卒中及颅内动脉再狭窄等。
1.4 统计学分析
采用SPSS 25.0统计学软件分析数据,计数资料以[n(%)]描述,比较采用χ2检验,计量资料以(x±s)描述,比较采用t检验,P < 0.05为差异有统计学意义。
2. 结果
2.1 治疗前后颅内动脉狭窄率比较
治疗前, 2组患者颅内动脉狭窄率比较,差异无统计学意义(P>0.05); 治疗后, 2组患者颅内动脉狭窄率均低于治疗前,且研究组低于对照组,差异有统计学意义(P < 0.05), 见表 1。
表 1 2组患者治疗前后颅内动脉狭窄率比较(x±s)% 组别 n 治疗前 治疗后 对照组 50 85.87±4.52 34.57±6.48* 研究组 50 85.23±5.47 12.32±3.26*# 与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。 2.2 治疗前后神经功能比较
治疗前, 2组患者NIHSS评分比较,差异无统计学意义(P>0.05); 治疗后, 2组患者NIHSS评分均低于治疗前,且研究组低于对照组,差异有统计学意义(P < 0.05), 见表 2。
表 2 2组患者治疗前后NIHSS评分比较(x±s)分 组别 n 治疗前 治疗后 对照组 50 26.19±5.54 9.91±1.65* 研究组 50 25.42±4.86 5.47±1.28*# NIHSS: 美国国立卫生研究院卒中量表。
与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。2.3 治疗前后日常生活能力比较
治疗前, 2组患者ADL评分比较,差异无统计学意义(P>0.05); 治疗后, 2组患者ADL评分均高于治疗前,且研究组高于对照组,差异有统计学意义(P < 0.05), 见表 3。
表 3 2组患者治疗前后ADL评分比较(x±s)分 组别 n 治疗前 治疗后 对照组 50 26.68±6.47 48.61±7.87* 研究组 50 27.43±4.51 60.97±6.75*# ADL: 日常生活活动能力量表。
与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。2.4 治疗前后脑血流灌注指标比较
治疗前, 2组患者PSV、搏动指数比较,差异无统计学意义(P>0.05); 治疗后, 2组患者PSV、搏动指数均低于治疗前,且研究组低于对照组,差异有统计学意义(P < 0.05), 见表 4。
表 4 2组患者治疗前后脑血流灌注指标比较(x±s)组别 n PSV/(cm/s) 搏动指数 治疗前 治疗后 治疗前 治疗后 对照组 50 169.82±27.86 114.34±17.72* 1.78±0.42 1.19±0.23* 研究组 50 167.95±24.34 87.85±14.63*# 1.75±0.34 0.81±0.17*# PSV: 狭窄段收缩期峰值流速。与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。 2.5 不良反应发生情况比较
研究组患者的不良反应发生率低于对照组,差异有统计学意义(P < 0.05), 见表 5。
表 5 2组患者不良反应发生情况比较[n(%)]组别 n 缺血性卒中 出血性卒中 颅内动脉再狭窄 合计 对照组 50 5(10.00) 1(2.00) 2(4.00) 8(16.00) 研究组 50 2(4.00) 0 1(2.00) 3(6.00)* 与对照组比较, * P < 0.05。 3. 讨论
卒中是导致人类残疾和死亡的主要原因之一,急性缺血性卒中约占全部卒中的80%[7-9], 治疗的关键在于尽早开通阻塞血管,挽救缺血半暗带[10-12]。sICAS是指由动脉粥样硬化引起的颅内动脉狭窄,且在狭窄动脉供血区域发生过缺血性卒中或短暂性脑缺血发作[13-15]。抗血小板治疗和降脂稳定斑块是sICAS的重要治疗手段,但部分患者接受规范药物治疗后仍会出现症状复发或病情进展。此外,口服抗血小板药物起效时间及持续时间较长,短时间内无法重复给药,且可能存在口服药物抵抗等现象,进一步加重了患者及其家属的身心负担及经济压力[16-17]。因此,探寻一种安全有效的治疗方法对于改善sICAS患者的预后具有重要意义。
随着医学技术的不断发展,血管内治疗(如支架置入、狭窄血管段球囊扩张等)已成为开通“罪犯”血管、提高远端血管支配区脑组织血液供应的重要手段,显著提升了sICAS患者的临床疗效[18-20]。目前,颅内动脉支架置入已被广泛应用于颈内动脉狭窄的治疗,并成为神经科研究的热点之一[21-22]。颅内动脉支架置入治疗能在短期内迅速改善大脑供血,为急性卒中的治疗提供了新方向。然而,支架内再狭窄仍是颅内支架置入术后的主要问题之一[23]。李振强等[24]回顾性分析15例重度sICAS患者的颅内支架置入情况,结果显示所有支架一次性释放成功,手术成功率为100%, 患者未出现缺血性卒中、短暂性脑缺血发作和颅内出血等情况,随访影像学资料显示仅1例患者发生支架内再狭窄,表明颅内支架置入治疗的成功率较高,并发症较少,且随访效果良好。
本研究结果显示,研究组患者治疗后颅内动脉狭窄率显著低于对照组,表明支架置入相较于药物治疗可显著降低狭窄率; 研究组患者治疗后NIHSS评分显著低于对照组,表明支架置入相较于药物治疗可显著改善患者神经功能; 研究组患者治疗后ADL评分显著高于对照组,表明支架置入相较于药物治疗可显著改善患者的日常生活活动能力; 研究组患者治疗后PSV和搏动指数显著低于对照组,表明支架置入相较于药物治疗可显著改善患者的脑血流灌注情况; 研究组患者的不良反应发生率显著低于对照组,表明支架置入相较于药物治疗可显著减少不良反应。
综上所述,血管内支架置入术治疗sICAS患者具有良好的有效性,能够显著降低颅内动脉狭窄率,改善患者的神经功能和日常生活活动能力,且安全性较高。
-
表 1 低体温组与正常体温组患者临床资料比较(x±s)[n(%)]
指标 分类 n 低体温组(n=195) 正常体温组(n=141) χ2/t P 年龄 ≤60岁 80 35(17.95) 45(31.91) 8.799 0.003 >60岁 256 160(82.05) 96(68.09) 性别 男 194 106(54.36) 88(63.41) 2.174 0.140 女 142 89(45.64) 53(37.59) 体质量指数 ≤22 kg/m2 134 83(42.56) 51(36.17) 1.395 0.238 >22 kg/m2 202 112(57.44) 90(63.83) 基础疾病史 有 224 137(70.26) 87(61.70) 2.695 0.101 无 112 58(29.74) 54(38.30) 术前体温/℃ — 36.52±0.12 36.55±0.17 1.896 0.059 手术室室温/℃ — 23.56±0.35 23.60±0.32 1.071 0.285 麻醉类型 全麻 152 83(42.56) 69(48.94) 1.341 0.247 全麻联合局麻 184 112(57.44) 72(51.06) 术中出血量 ≤60 mL 173 83(42.56) 90(63.83) 14.816 < 0.001 >60 mL 163 112(57.44) 51(36.17) 液体输入量 ≤1 000 mL 157 72(36.92) 85(60.28) 4.080 0.043 >1 000 mL 179 123(63.08) 56(39.72) 输入液体温度/℃ — 36.09±0.13 36.12±0.16 1.893 0.059 手术时间 ≤2.5 h 163 82(42.05) 81(57.45) 7.765 0.005 >2.5 h 173 113(57.95) 60(42.55) 表 2 腔镜下甲状腺癌根治术术中低体温的多因素Logistic回归分析
变量 β SE Wald P OR 95%CI 年龄 0.604 0.275 4.836 0.028 1.829 1.068~3.133 术中出血量 0.549 0.246 4.983 0.026 1.731 1.069~2.802 液体输入量 0.645 0.243 7.057 0.008 1.906 1.184~3.067 手术时间 0.557 0.244 5.212 0.022 1.745 1.082~2.815 常量 -1.001 0.281 12.669 < 0.001 0.367 — -
[1] 李英杰, 王芳, 卢想. 麻醉诱导前给予咪达唑仑对甲状腺癌根治术患者E、NE及IL-10水平的影响[J]. 解放军医药杂志, 2022, 34(2): 44-47. https://www.cnki.com.cn/Article/CJFDTOTAL-HBGF202202010.htm [2] 汲权威. 完全腔镜下甲状腺癌根治术对患者机体应激反应、预后的影响分析[J]. 四川解剖学杂志, 2020, 28(1): 61-62, 74. https://www.cnki.com.cn/Article/CJFDTOTAL-SCGP202001029.htm [3] 杜德良, 王红. 全腔镜甲状腺癌根治术与传统开放手术的临床效果分析[J]. 腹腔镜外科杂志, 2022, 27(6): 406-409. https://www.cnki.com.cn/Article/CJFDTOTAL-FQJW202206002.htm [4] ZOU B W, TU Y, LIAO D W, et al. Radical esophagectomy for stage Ⅱ and Ⅲ thoracic esophageal squamous cell carcinoma followed by adjuvant radiotherapy with or without chemotherapy: which is more beneficial[J]. Thorac Cancer, 2020, 11(3): 631-639. doi: 10.1111/1759-7714.13307
[5] 史卓颖, 张海伟, 杜祥飞. 全身麻醉病人术中低体温发生预测模型的建立[J]. 护理研究, 2021, 35(2): 246-249. https://www.cnki.com.cn/Article/CJFDTOTAL-SXHZ202102010.htm [6] 王杰, 马雪松, 樊桂波, 等. 围术期体温监测及保温的现状分析[J]. 现代生物医学进展, 2019, 19(3): 583-586. https://www.cnki.com.cn/Article/CJFDTOTAL-SWCX201903045.htm [7] DENDIS M, HOOVEN K. Preventing hypothermia during cesarean birth: an integrative review[J]. MCN Am J Matern Child Nurs, 2020, 45(2): 102-108. doi: 10.1097/NMC.0000000000000599
[8] 海洁, 白立炜, 王艾蒙. 围手术期多学科协作对甲状腺癌根治术患者术后恢复、负性情绪的影响[J]. 癌症进展, 2022, 20(2): 196-199. https://www.cnki.com.cn/Article/CJFDTOTAL-AZJZ202202026.htm [9] 费阳, 李阳, 陈峰, 等. 完全腔镜甲状腺癌根治术对患者创伤应激与免疫的影响[J]. 腹腔镜外科杂志, 2022, 27(7): 483-486. https://www.cnki.com.cn/Article/CJFDTOTAL-FQJW202207002.htm [10] 岳璇弟, 刘文亚, 向玲, 等. 全腔镜甲状腺切除术治疗分化型甲状腺癌的效果及复发危险因素分析[J]. 解放军医药杂志, 2021, 33(6): 30-34. https://www.cnki.com.cn/Article/CJFDTOTAL-HBGF202106007.htm [11] 白海燕, 周建玲, 张莹, 等. 儿童术中低体温对凝血功能、炎症反应和术后感染发生的影响及术中低体温危险因素分析[J]. 临床和实验医学杂志, 2022, 21(24): 2650-2654. https://www.cnki.com.cn/Article/CJFDTOTAL-SYLC202224020.htm [12] 鲍加玉, 李海龙, 温儒民. 术中低温对肌层浸润性膀胱癌行腹腔镜膀胱根治性切除术后并发症及预后的影响[J]. 中国临床医生杂志, 2021, 49(1): 82-84. https://www.cnki.com.cn/Article/CJFDTOTAL-ZLYS202101026.htm [13] GUNDERSEN S K, MEYHOFF C S, WETTERSLEV J, et al. The impact of intraoperative fluid therapy and body temperature on surgical site infection-reassessment of a randomized trial[J]. Chirurgia, 2018, 113(4): 516-523. doi: 10.21614/chirurgia.113.4.516
[14] GALA T, SHAHZAD N, EDHI A I, et al. Perioperative hypothermia in colorectal surgeries: are we doing enough to prevent it[J]. J Pak Med Assoc, 2020, 70(2): 304-307.
[15] 宁红岩, 王颖, 陈辰, 等. 加热措施对腹腔镜手术患者影响的研究[J]. 中国实用护理杂志, 2019, 35(33): 2584-2587. https://www.cnki.com.cn/Article/CJFDTOTAL-JHSY202312014.htm [16] 林文慧, 张秀贤, 黄爱虹. 围术期一体化保温护理模式对妇科腔镜手术患者的影响[J]. 齐鲁护理杂志, 2021, 27(16): 139-142. https://www.cnki.com.cn/Article/CJFDTOTAL-QLHL202116059.htm [17] 袁培培, 魏晓宇, 王宁. 保温护理对妇科腹腔镜手术患者术后低体温与寒战的预防效果[J]. 护理实践与研究, 2020, 17(21): 122-123. https://www.cnki.com.cn/Article/CJFDTOTAL-HLSJ202021049.htm [18] 成紫琳, 马靓. 开颅手术继发术中低体温的风险模型构建及复合保温措施干预研究[J]. 医学综述, 2021, 27(20): 4150-4155. https://www.cnki.com.cn/Article/CJFDTOTAL-YXZS202120033.htm [19] 孙亮, 高倩, 王广, 等. 麻醉后恢复室期间全身麻醉患者发生低体温的影响因素[J]. 中华医学杂志, 2021, 101(1): 52-56. [20] OKADA N, FUJITA T, KANAMORI J, et al. Efficacy of prewarming prophylaxis method for intraoperative hypothermia during thoracoscopic esophagectomy[J]. Esophagus, 2020, 17(4): 385-391. doi: 10.1007/s10388-020-00743-8
[21] 魏勇, 代德珍, 王辉. 无缝衔接整体干预对重症胰腺炎腹腔镜手术患者术中低体温及预后的影响[J]. 实用医院临床杂志, 2021, 18(4): 185-188. https://www.cnki.com.cn/Article/CJFDTOTAL-YYLC202104054.htm [22] LI Y N, LIANG H S, FENG Y. Prevalence and multivariable factors associated with inadvertent intraoperative hypothermia in video-assisted thoracoscopic surgery: a single-center retrospective study[J]. BMC Anesthesiol, 2020, 20(1): 25. doi: 10.1186/s12871-020-0953-x
[23] 李丽, 颜艳, 房馨, 等. 腹腔镜手术患者术中低体温风险预测模型的构建及验证[J]. 中华护理杂志, 2022, 57(4): 463-468. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHHL202204012.htm




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
